Un nou tip de model de computer care poate dezvălui daunele radiațiilor la nivel celular ar putea îmbunătăți rezultatele radioterapiei pentru pacienții cu cancer pulmonar.
Roman Bauer, un neuroștiință computațional la Universitatea din Surrey în Marea Britanie, în colaborare cu Mark în timpul și Nicolò Cogno din GSI Helmholtzzentrum für Schwerionenforschung în Germania, a creat modelul, care simulează modul în care radiațiile interacționează cu plămânii, celulă cu celulă.
Peste jumătate din toți pacienții cu cancer pulmonar sunt tratați prin radioterapie. Deși această abordare este eficientă, lasă până la 30% dintre primitori cu leziuni induse de radiații. Acestea pot declanșa afecțiuni grave care afectează respirația, cum ar fi fibroza – în care căptușeala alveolelor (sacii de aer) din plămâni este îngroșată și rigidizată – și pneumonita – când pereții alveolelor devin inflamate.
Pentru a limita daunele cauzate de radiații la țesutul sănătos, în același timp uciderea celulelor canceroase, radioterapia este administrată în mai multe „fracții” separate. Acest lucru permite o doză mai mare – și, prin urmare, mai eficientă – să fie administrată în general, deoarece unele dintre celulele sănătoase deteriorate se pot repara singure între fiecare fracție.
În prezent, schemele de fracționare a radioterapiei sunt alese pe baza experienței anterioare și a modelelor statistice generalizate, deci nu sunt optimizate pentru pacienți individuali. În schimb, medicina personalizată ar putea fi realizată datorită acestui nou model care, după cum a spus Durante, director al Departamentul de Biofizică la GSI explică, analizează „toxicitatea în țesuturi pornind de la reacțiile celulare de bază și, prin urmare, este capabil să prezică ce se întâmplă cu orice pacient” atunci când sunt alese diferite scheme de fracționare.
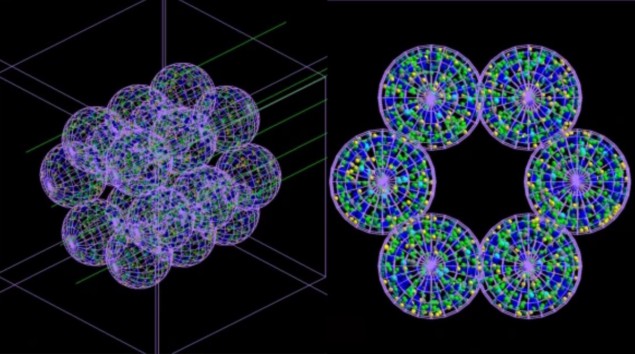
Echipa a dezvoltat un model „bazat pe agenți” (ABM) constând din unități sau agenți care interacționează separat – care în acest caz imită celulele pulmonare – cuplat cu un simulator Monte Carlo. ABM, descris în Medicina Comunicațiilor, construiește o reprezentare a unui segment alveolar format din 18 alveole fiecare cu diametrul de 260 µm. Apoi, simulări Monte Carlo ale iradierii acestor alveole sunt efectuate la scară microscopică și nanoscopică, iar informațiile despre doza de radiație livrată fiecărei celule și distribuția acesteia sunt reintroduse în ABM.
ABM folosește aceste informații pentru a determina dacă fiecare celulă va trăi sau va muri și emite rezultatele finale sub forma unei imagini 3D. În mod esențial, modelul cuplat poate simula trecerea timpului și, astfel, arăta severitatea daunelor cauzate de radiații – și progresia afecțiunilor medicale pe care le poate provoca – la ore, zile, luni sau chiar ani după tratament.
„Ceea ce mi s-a părut foarte interesant este că aceste simulări computaționale au furnizat de fapt rezultate care se potriveau cu diferite observații experimentale de la diferite grupuri, laboratoare și spitale. Deci abordarea noastră computațională ar putea fi, în principiu, utilizată într-un cadru clinic”, spune Bauer, purtătorul de cuvânt al organizației internaționale. Colaborare BioDynaMo, care își propune să aducă noi metode de calcul în asistența medicală prin intermediul suitei de software utilizate pentru a construi acest model.
Bauer a început să lucreze la modele computaționale de cancer după ce un prieten apropiat a murit din cauza bolii la doar 34 de ani. „Fiecare cancer este diferit și fiecare persoană este diferită, cu organe de formă, predispoziții genetice și stiluri de viață diferite”, explică el. Speranța lui este că informațiile din scanări, biopsii și alte teste ar putea fi introduse în noul model pentru a oferi o imagine a fiecărui individ. Ar putea fi apoi creat un protocol de terapie asistată de IA, care ar produce un plan de tratament adaptat îndeaproape, care îmbunătățește șansele de supraviețuire ale pacientului.
Planificarea specifică pacientului ar putea îmbunătăți rezultatele radioterapiei
Bauer caută în prezent colaboratori din alte discipline, inclusiv fizica, pentru a ajuta la trecerea la un studiu clinic care urmărește pacienții cu cancer pulmonar de-a lungul mai multor ani. Între timp, echipa intenționează să extindă utilizarea modelului în alte domenii ale medicinei.
Durante, de exemplu, speră să studieze infecția virală cu acest model pulmonar, deoarece „poate prezice pneumonita indusă de infecția cu COVID-19”. Între timp, Bauer a început să simuleze dezvoltarea circuitelor în creierul bebelușilor prematuri, cu scopul de a înțelege mai bine „în ce moment să intervină și cum”.
- Distribuție de conținut bazat pe SEO și PR. Amplifică-te astăzi.
- PlatoData.Network Vertical Generative Ai. Împuterniciți-vă. Accesați Aici.
- PlatoAiStream. Web3 Intelligence. Cunoștințe amplificate. Accesați Aici.
- PlatoESG. carbon, CleanTech, Energie, Mediu inconjurator, Solar, Managementul deșeurilor. Accesați Aici.
- PlatoHealth. Biotehnologie și Inteligență pentru studii clinice. Accesați Aici.
- Sursa: https://physicsworld.com/a/modelling-lung-cells-could-help-personalize-radiotherapy/
- :are
- :este
- :nu
- $UP
- 135
- 3d
- a
- Capabil
- Despre Noi
- AC
- realizat
- de fapt
- administrată
- afecta
- După
- în vârstă de
- agenţi
- isi propune
- AIR
- TOATE
- permite
- Cu toate ca
- an
- și
- Orice
- abordare
- SUNT
- domenii
- AS
- At
- înapoi
- bazat
- de bază
- bază
- BE
- deoarece
- deveni
- început
- început
- Mai bine
- între
- respiraţie
- aduce
- construi
- construiește
- by
- CAN
- Rac
- Celule canceroase
- transportate
- caz
- Provoca
- celulă
- Celule
- șansele
- ales
- clinic
- Închide
- îndeaproape
- colaborare
- colaboratori
- de calcul
- calculator
- Condiții
- Constând
- contrast
- ar putea
- cuplat
- Covid-19
- a creat
- crucial
- În prezent
- prejudiciu
- Zi
- livrate
- Departament
- descris
- dezvoltat
- Dezvoltare
- .
- decedat
- diferit
- Director
- discipline
- Boală
- distribuire
- doză
- fiecare
- Eficace
- Chiar
- Fiecare
- captivant
- Extinde
- experienţă
- experimental
- explică
- fed-
- final
- următor
- Pentru
- formă
- găsit
- fracțiune
- prieten
- din
- generalizată
- genetic
- Germania
- scop
- Grupului
- Jumătate
- se întâmplă
- he
- de asistență medicală
- sănătos
- ajutor
- superior
- lui
- speranţă
- sperând
- spitale
- ORE
- Cum
- HTTPS
- i
- îmbunătăţi
- îmbunătăţeşte
- in
- Inclusiv
- individ
- informații
- leziuni
- instanță
- intenționează
- interacționând
- interactiv
- Internațional
- interveni
- în
- problema
- IT
- ESTE
- jpg
- doar
- ucidere
- Labs
- Nivel
- stiluri de viață
- LIMITĂ
- căptuşeală
- trăi
- Se pare
- potrivire
- max-width
- Mai..
- Între timp
- medical
- medicină
- Metode
- microscopic
- model
- modelare
- Modele
- luni
- mai mult
- muta
- Natură
- Nou
- următor
- of
- on
- optimizate
- or
- comandă
- Altele
- al nostru
- afară
- rezultate
- producție
- iesiri
- peste
- global
- trecere
- trecut
- pacient
- pacientes
- persoană
- personaliza
- Personalizat
- Fizică
- Lumea fizicii
- imagine
- plan
- planificare
- Plato
- Informații despre date Platon
- PlatoData
- Punct
- prezice
- Prematur
- principiu
- progresie
- protocol
- furniza
- Radioterapie
- Reacții
- destinatari
- repara
- reprezentare
- REZULTATE
- dezvălui
- spune
- Scară
- scanări
- scheme
- caută
- segment
- distinct
- serios
- instalare
- câteva
- profilat
- Arăta
- simula
- simulări
- Simulator
- So
- Software
- unele
- Purtatorul de cuvant al
- Pornire
- statistic
- Încă
- Studiu
- astfel de
- suită
- Surrey
- supravieţuire
- adaptate
- echipă
- teste
- mulțumesc
- acea
- Marea Britanie
- se
- apoi
- terapie
- prin urmare
- Acestea
- acest
- miniatura
- Prin urmare
- timp
- la
- față de
- tratate
- tratament
- proces
- declanşa
- adevărat
- tip
- Uk
- înţelegere
- de unităţi
- utilizare
- utilizat
- utilizări
- folosind
- diverse
- foarte
- de
- virale
- Ce
- cand
- dacă
- care
- în timp ce
- cu
- în
- Apartamente
- a face exerciţii fizice
- de lucru
- lume
- ar
- ani
- zephyrnet