Tratarea cancerului cu radiații poate stimula răspunsul imunitar al organismului și poate inhiba creșterea tumorii, dar poate reduce și nivelul limfocitelor, celulelor albe din sânge asociate cu răspunsul imun, ceea ce duce la afectarea controlului tumorii și la prognostic prost. Severitatea acestei limfopenii induse de radiații se corelează cu doza administrată celulelor sanguine și limfocitelor circulante. Ca atare, reducerea la minimum a dozei către inimă, sângele periferic și organele limfoide ar putea ajuta la reducerea acestui efect dăunător.
Pentru a investiga în continuare această teorie, Antje Galts și Abdelkhalek Hammi de la Universitatea TU Dortmund a explorat dacă radioterapia FLASH - radiații livrate la doze ultra-înalte - ar putea reduce nivelul de epuizare a celulelor imune în timpul terapiei cu protoni a pacienților cu cancer cerebral.
„Mecanismul biologic din spatele efectului de economisire a FLASH observat la doze mari nu este încă pe deplin înțeles. Cu toate acestea, una dintre teoriile propuse este ipoteza imunitară, care sugerează că livrarea instantanee a dozei de iradiere FLASH reduce semnificativ epuizarea limfocitelor circulante prin reducerea la minimum a timpului de expunere”, explică Hammi. „În studiul nostru, am arătat că un tratament hipofracționat și livrarea rapidă a dozei au scutit celulele imune de până la 27 de ori, comparativ cu un plan de tratament convențional cu scanare cu fascicul de protoni fracționați.”
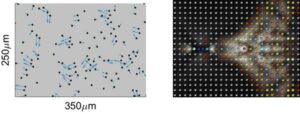
Galts și Hammi au folosit a modelul dozimetric al fluxului sanguin pentru a simula doza la limfocitele circulante în timpul terapiei cu protoni cu intensitate modulată (IMPT) convențională și bazată pe FLASH a unei tumori cerebrale. Modelul de livrare dinamică a fasciculului simulează un plan de tratament fracționat IMPT, luând în considerare variația spațio-temporală a ratei de doză a fiecărui fascicul creion de protoni. Hammi observă că modelul încorporează parametri realiști de livrare de la ciclotronii disponibili comercial.
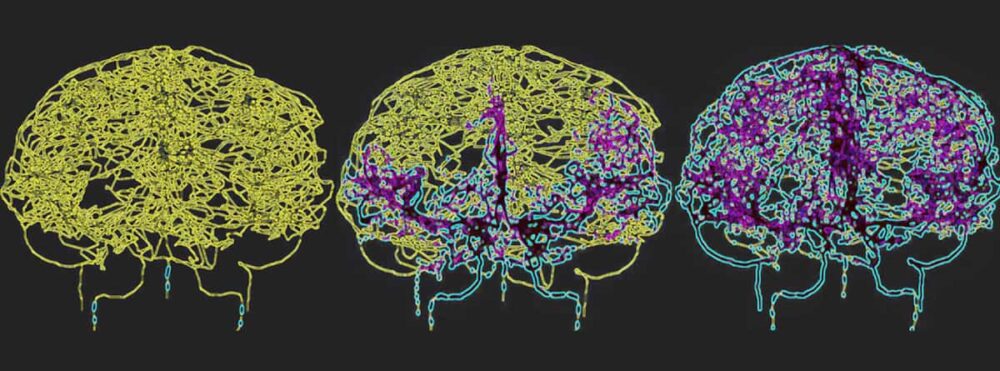
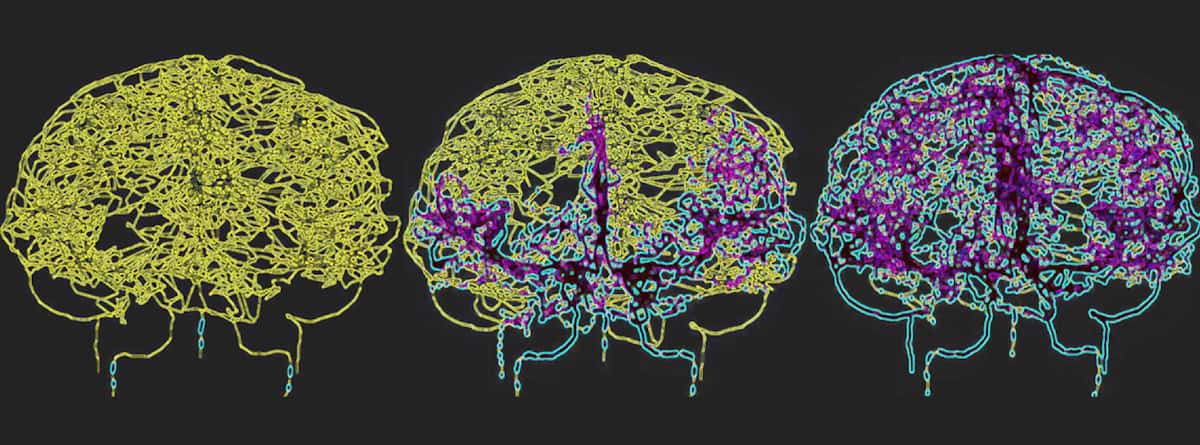
Pentru a reflecta cu acuratețe circulația sângelui în creierul uman, Galts și Hammi au cartografiat vasele de sânge direct din imaginile angiografice MR ale creierului. Ei au folosit modelul cerebrovascular rezultat, care a inclus 465 de vase de sânge și 8841 de ramuri de vase individuale, pentru a simula circulația celulelor imune în fluxul sanguin.
Cercetătorii au creat planuri realiste de tratament IMPT pentru o tumoare de glioblastom, folosind patru fascicule de protoni incidente și parametri de livrare relevanți clinic. Apoi au calculat câmpurile de radiații care variază în timp la care este expus sângele circulant în timpul administrării planurilor de terapie cu protoni și doza acumulată după tratament, raportând constatările lor în Fizica în medicină și biologie.
Glioblastomul este cea mai letală formă de cancer cerebral, iar tratarea acesteia cu radioterapie poate provoca limfopenie prelungită indusă de radiații. „Prin modelarea unui sistem cerebrovascular în timpul administrării radiațiilor, sperăm să obținem o perspectivă mai profundă asupra modului în care radioterapia afectează răspunsul imun la aceste grupuri de pacienți, ceea ce poate duce la strategii terapeutice îmbunătățite”, spune Hammi.
Planificați comparații
Galts și Hammi au examinat patru scenarii de tratament: IMPT FLASH cu o singură fracțiune de 22.3 Gy; FLASH hipofracționat folosind două fracții de 14.6 Gy și cinci fracții de 8 Gy; și IMPT convențional folosind treizeci și două de fracții de 2 Gy. Pentru fiecare plan de tratament, ei au evaluat impactul dozimetric asupra limfocitelor circulante și au estimat radiotoxicitatea rezultată.
Histogramele doză-volum au arătat că radioterapia FLASH a redus semnificativ proporția de celule iradiate în comparație cu rata convențională a dozei IMPT. În timpul primei fracțiuni de tratament, toate cele trei scheme FLASH au iradiat aproximativ 1.52% din volumul sanguin circulant, în timp ce IMPT convențional a iradiat 2.18%. Planurile FLASH hipofracționate, livrate în două sau cinci fracții, au crescut acest volum iradiat la 3.01% și, respectiv, 7.35%, în timp ce IMPT convențional a expus 42.41% din sângele periferic la radiații.
În continuare, cercetătorii au examinat nivelul de limfocite circulante care au primit o doză de cel puțin 7 cGy - un prag care provoacă o depleție de 2% în populația de limfocite - pe parcursul întregului tratament. După finalizarea IMPT convențională, 25.65% din limfocitele circulante au primit o doză de cel puțin 7 cGy. Pentru tratamentele FLASH cu o singură, două și cinci fracțiuni, volumele care au primit mai mult decât acest prag de doză au fost de 1.21%, 2.30% și, respectiv, 5.14%.
Volumele de limfocite circulante care au primit doze de peste 100 cGy, care provoacă o depleție de 30%, au fost de 0.77%, 1.28% și 2.09% pentru FLASH cu o singură, două și, respectiv, cinci fracțiuni și 0.10% în timpul IMPT convențional.
Galts și Hammi au studiat, de asemenea, răspunsul limfocitelor CD4+ și CD8+, care au distribuții diferite în sângele periferic, la diferitele scenarii de iradiere. Pentru ambele tipuri de limfocite, distrugerea celulelor după prima fracțiune a fost de 0.66%, 0.62%, 0.32% și 0.08% pentru FLASH cu o singură, două și cinci fracțiuni și, respectiv, IMPT convențional.
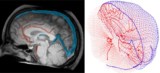
Modelul computațional determină doza la sânge în timpul radioterapiei
După tratamentul complet, epuizarea limfocitelor a fost de 1.02% și 1.56% pentru fracțiunile cu două și, respectiv, cinci tratamente și 2.14% pentru IMPT convențional. Aceste descoperiri demonstrează că terapia cu protoni FLASH scutește celulele imune circulante în timpul tratamentului intracranian, FLASH cu o singură fracțiune reducând rata de epuizare cu aproape 70% în comparație cu IMPT convențional.
spune Hammi Lumea fizicii că acum extind modelul pentru a include cancere de cap și gât. „În plus, explorăm diferite metode de livrare FLASH și impactul acestora asupra epuizării sistemului imunitar, cu un accent deosebit pe tratamentul FLASH conform care se bazează pe modularea pasivă, specifică pacientului, a energiei”, explică el. „Acest model de livrare are potențialul de a economisi mai multe limfocite circulante în comparație cu livrarea FLASH prin injectare.”
- Distribuție de conținut bazat pe SEO și PR. Amplifică-te astăzi.
- PlatoData.Network Vertical Generative Ai. Împuterniciți-vă. Accesați Aici.
- PlatoAiStream. Web3 Intelligence. Cunoștințe amplificate. Accesați Aici.
- PlatoESG. carbon, CleanTech, Energie, Mediu inconjurator, Solar, Managementul deșeurilor. Accesați Aici.
- PlatoHealth. Biotehnologie și Inteligență pentru studii clinice. Accesați Aici.
- Sursa: https://physicsworld.com/a/flash-irradiation-spares-immune-cells-during-proton-therapy/
- :are
- :este
- :nu
- $UP
- 1
- 10
- 100
- 14
- 160
- 2%
- 22
- 25
- 27
- 35%
- 7
- 8
- a
- acumulate
- precis
- După
- TOATE
- aproape
- de asemenea
- an
- și
- SUNT
- în jurul
- AS
- evaluat
- asociate
- At
- disponibil
- bazat
- Grindă
- în spatele
- sânge
- atât
- Creier
- cancer la creier
- ramuri
- dar
- by
- calculată
- CAN
- Rac
- Provoca
- cauze
- celulă
- Celule
- circulant
- Circulație
- clic
- comercial
- comparație
- completarea
- luand in considerare
- Control
- convențional
- ar putea
- a creat
- Mai adânc
- livrate
- livrare
- demonstra
- determină
- diferit
- direct
- distribuire
- distribuții
- doză
- dozele
- în timpul
- dinamic
- fiecare
- efect
- energie
- Întreg
- egal
- Echilibru
- estimativ
- extinderea
- explică
- explorat
- Explorarea
- expus
- Expunere
- FAST
- Domenii
- constatările
- First
- cinci
- bliț
- debit
- Concentra
- următor
- Pentru
- formă
- patru
- fracțiune
- din
- Complet
- complet
- mai mult
- Câştig
- Grupului
- Creștere
- Avea
- he
- inimă
- ajutor
- Înalt
- speranţă
- Cum
- Totuși
- HTTPS
- uman
- imagine
- imagini
- Sistem imunitar
- Impactul
- îmbunătățit
- IMPOZIT
- in
- incident
- include
- inclus
- încorporează
- a crescut
- individ
- informații
- perspective
- în
- investiga
- problema
- IT
- jpg
- ucidere
- conducere
- cel mai puțin
- stânga
- Nivel
- mai lung
- max-width
- mecanism
- medicină
- Metode
- minimizând
- model
- modelare
- modelare
- mai mult
- cele mai multe
- mr
- notițe
- acum
- of
- on
- ONE
- deschide
- or
- al nostru
- afară
- peste
- parametrii
- special
- pasiv
- pacientes
- Fizică
- Lumea fizicii
- plan
- Planurile
- Plato
- Informații despre date Platon
- PlatoData
- sărac
- populație
- potenţial
- potenţial
- proporție
- propus
- Radioterapie
- rată
- tarife
- realist
- primit
- primire
- reduce
- Redus
- reduce
- reducerea
- reflecta
- Raportarea
- cercetători
- respectiv
- răspuns
- rezultând
- Dezvăluit
- dreapta
- s
- spune
- scanare
- scenarii
- scheme
- a arătat
- semnificativ
- singur
- Începe
- stimula
- strategii
- curent
- studiat
- Studiu
- astfel de
- sugerează
- sistem
- spune
- decât
- acea
- lor
- apoi
- teorie
- terapie
- Acestea
- ei
- acest
- trei
- prag
- Prin
- miniatura
- timp
- ori
- la
- tratare
- tratament
- tratamente
- adevărat
- Două
- Tipuri
- înțeles
- universitate
- utilizat
- folosind
- diverse
- Navă
- volum
- volume
- a fost
- we
- au fost
- cand
- dacă
- care
- în timp ce
- alb
- cu
- în
- lume
- încă
- zephyrnet