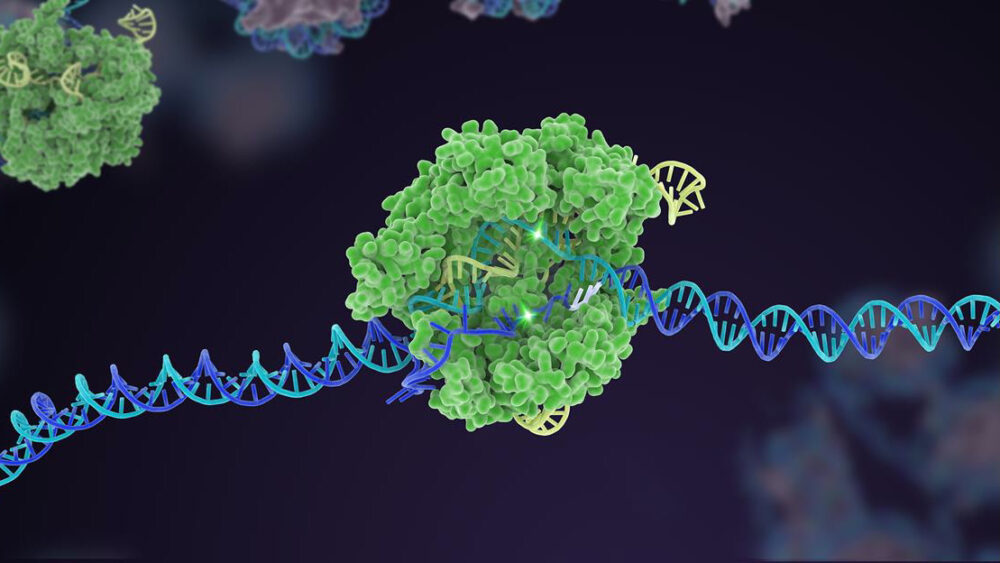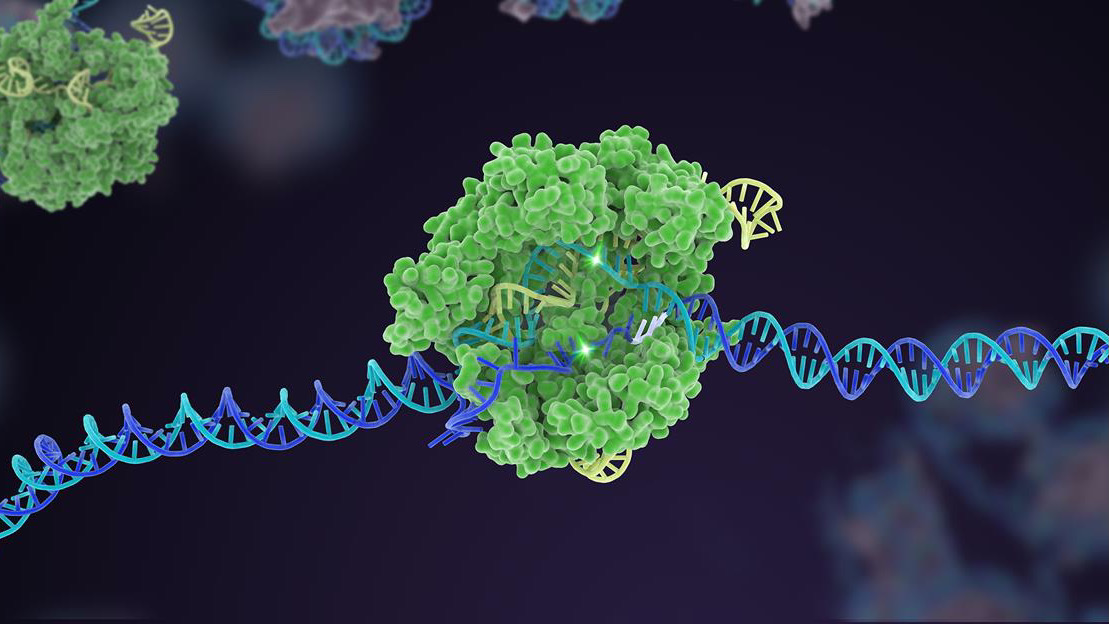
För tio år sedan sköt en föga känd bakteriell försvarsmekanism i höjden till berömmelse som en kraftfull genomredigerare. Under decenniet sedan dess har CRISPR-Cas9 skapat flera varianter och expanderat till en omfattande verktygslåda som kan redigera livets genetiska kod.
Långt ifrån en strävan efter elfenbenstorn, dess praktiska användningar inom forskning, sjukvård och jordbruk kom snabbt och rasande.
Du har sett rubrikerna. FDA godkände dess användning i ta itu med den underliggande genetiska mutationen för sicklecellssjukdom. Några forskare redigerade immunceller för att bekämpa obehandlad blodcancer hos barn. Andra tog organtransplantationer från gris till människa från dröm till verklighet i ett försök att lindra bristen på donatororgan. Det senaste arbetet syftar till att hjälpa miljontals människor med högt kolesterol – och potentiellt ge CRISPR-baserad genterapi till massorna – genom att sänker deras chanser att drabbas av hjärtsjukdomar med en enda injektion.
Men till Dr Jennifer Doudna, som vann Nobelpriset 2020 för sin roll i att utveckla CRISPR, vi skrapar bara på ytan av dess potential. Tillsammans med doktoranden Joy Wang lade Doudna en färdplan för teknikens nästa decennium i en artikel in Vetenskap.
Om 2010-talet var fokuserat på att etablera CRISPR-verktygslådan och bevisa dess effektivitet, är detta decennium när tekniken når sin fulla potential. Från CRISPR-baserade terapier och storskaliga undersökningar för sjukdomsdiagnostik till konstruktion av högavkastande grödor och näringsrik mat, tekniken "och dess potentiella inverkan är fortfarande i ett tidigt skede", skrev författarna.
Ett decennium av höjdpunkter
Vi har spillt mycket bläck på CRISPR-framsteg, men det lönar sig att återvända till det förflutna för att förutsäga framtiden – och potentiellt spana efter problem på vägen.
En tidig höjdpunkt var CRISPRs otroliga förmåga att snabbt konstruera djurmodeller av sjukdomar. Dess ursprungliga form klipper lätt bort en riktad gen i ett mycket tidigt embryo, som när det transplanteras in i en livmoder kan generera genetiskt modifierade möss på bara en månad, jämfört med ett år med tidigare metoder. Ytterligare CRISPR-versioner, som basredigering - att byta ut en genetisk bokstav mot en annan - och prime redigering - som klipper DNA:t utan att klippa båda strängarna - stärkte ytterligare verktygslådans flexibilitet vid konstruktion av genetiskt förändrade organoider (tänk minihjärnor) och djur. CRISPR etablerade snabbt dussintals modeller för några av våra mest förödande och förvirrande sjukdomar, inklusive olika cancerformer, Alzheimers och Duchennes muskeldystrofi – en degenerativ sjukdom där muskeln långsamt försvinner. Dussintals CRISPR-baserade försök finns nu i arbetena.
CRISPR accelererade också genetisk screening in i big data-åldern. Istället för att rikta in sig på en gen i taget, är det nu möjligt att tysta, eller aktivera, tusentals gener parallellt, vilket bildar en sorts Rosetta-sten för att översätta genetiska störningar till biologiska förändringar. Detta är särskilt viktigt för att förstå genetiska interaktioner, såsom de i cancer eller åldrande som vi inte tidigare var insatta i, och för att få ny ammunition för läkemedelsutveckling.
Men en krona på verket för CRISPR var multiplexed redigering. Som att samtidigt knacka på flera pianotangenter, riktar den här typen av genteknik sig till flera specifika DNA-områden, och förändrar snabbt ett genoms genetiska sammansättning på en gång.
Tekniken fungerar i växter och djur. I evigheter har människor mödosamt förädlat grödor med önskvärda egenskaper – vare sig det är färg, storlek, smak, näring eller motståndskraft mot sjukdomar. CRISPR kan hjälpa till att välja efter flera egenskaper eller till och med tämja nya grödor på bara en generation. CRISPR-genererade hornlösa tjurar, näringsrika tomater, och hypermuskulära husdjur och fisk redan är verklighet. Med världens befolkning upp till 8 miljarder 2022 och miljoner som lider av hunger, CRISPRed-grödor kan ge en livlina – det vill säga om människor är villiga att acceptera tekniken.
Vägen framåt
Var ska vi gå härifrån?
För författarna måste vi ytterligare öka CRISPRs effektivitet och bygga förtroende. Detta innebär att gå tillbaka till grunderna för att öka verktygets redigeringsnoggrannhet och precision. Här är plattformar för att snabbt utveckla Cas-enzymer, "sax"-komponenten i CRISPR-maskineriet, avgörande.
Det har redan varit framgångar: en Cas-version, till exempel, fungerar som ett skyddsräcke för målkomponenten - sgRNA "blodhund". I klassisk CRISPR fungerar sgRNA:t ensamt, men i denna uppdaterade version kämpar det för att binda utan Cas-hjälp. Det här tricket hjälper till att skräddarsy redigeringen till en specifik DNA-plats och ökar noggrannheten så att skärningen fungerar som förutspått.
Liknande strategier kan också öka precisionen med färre biverkningar eller infoga nya gener i celler som neuroner och andra som inte längre delar sig. Även om det redan är möjligt med prime-redigering, kan dess effektivitet vara 30 gånger lägre än klassiska CRISPR-mekanismer.
"Ett huvudmål för prime-redigering under det kommande decenniet är att förbättra effektiviteten utan att kompromissa med redigeringsproduktens renhet - ett resultat som har potential att förvandla prime-redigering till ett av de mest mångsidiga verktygen för precisionsredigering", sa författarna.
Men kanske viktigare är leverans, som förblir en flaskhals, särskilt för terapeutika. För närvarande används CRISPR i allmänhet på celler utanför kroppen som infunderas tillbaka – som i fallet med CAR-T – eller i vissa fall bundna till en virusbärare eller inkapslade i fettbubblor och injiceras i kroppen. Det har varit framgångar: i 2021, godkände FDA första CRISPR-baserade skottet för att tackla en genetisk blodsjukdom, transtyretinamyloidos.
Ändå är båda strategierna problematiska: inte många typer av celler kan överleva CAR-T-behandlingen - dör när de återinförs i kroppen - och inriktning på specifika vävnader och organ förblir oftast utom räckhåll för injicerbara terapier.
Ett viktigt framsteg för det kommande decenniet, sa författarna, är att transportera CRISPR-lasten in i den riktade vävnaden utan att skada och släppa genredigeraren på den avsedda platsen. Vart och ett av dessa steg, även om det verkar enkla på pappret, presenterar sin egen uppsättning utmaningar som kommer att kräva både bioteknik och innovation för att övervinna.
Slutligen kan CRISPR synergisera med andra tekniska framsteg, sa författarna. Till exempel, genom att utnyttja cellavbildning och maskininlärning, skulle vi snart kunna konstruera ännu mer effektiva genomredigerare. Tack vare snabbare och billigare DNA-sekvensering, kan vi sedan enkelt övervaka konsekvenserna av genredigering. Dessa data kan sedan tillhandahålla en slags återkopplingsmekanism för att konstruera ännu mer kraftfulla genomredigerare i en virtuous loop.
Verkliga inverkan på världen
Även om ytterligare utbyggnad av CRISPR-verktygslådan står på agendan, är tekniken tillräckligt mogen för att påverka den verkliga världen under sitt andra decennium, sa författarna.
Inom en snar framtid borde vi se "ett ökat antal CRISPR-baserade behandlingar som flyttar till senare stadier av kliniska prövningar." Om man ser längre fram, kan tekniken, eller dess varianter, göra xenotransplantationer från gris till människa till rutin snarare än experimentella. Storskaliga undersökningar av gener som leder till åldrande eller degenerativa hjärn- eller hjärtsjukdomar – våra främsta mördare idag – skulle kunna ge profylaktiska CRISPR-baserade behandlingar. Det är ingen lätt uppgift: vi behöver både kunskap om genetiken bakom mångfacetterade genetiska sjukdomar – det vill säga när flera gener spelar in – och ett sätt att leverera redigeringsverktygen till deras mål. "Men de potentiella fördelarna kan driva innovation inom dessa områden långt utöver vad som är möjligt idag," sa författarna.
Men med större makt kommer större ansvar. CRISPR har avancerat i rasande fart, och tillsynsmyndigheter och allmänheten kämpar fortfarande för att komma ikapp. Det kanske mest ökända exemplet var det CRISPR-barn, där experiment utförs mot globala etiska riktlinjer drivs ett internationellt konsortium för att fastställa en röd linje för redigering av mänskliga könsceller.
På samma sätt är genetiskt modifierade organismer (GMO) fortfarande ett kontroversiellt ämne. Även om CRISPR är mycket mer exakt än tidigare genetiska verktyg, är det upp till konsumenterna att bestämma om de vill välkomna en ny generation av mänskligt utvecklade livsmedel– både växter och djur.
Dessa är viktiga samtal som behöver global diskurs när CRISPR går in på sitt andra decennium. Men för författarna ser framtiden ljus ut.
"Precis som under tillkomsten av CRISPR-genomredigering kommer en kombination av vetenskaplig nyfikenhet och viljan att gynna samhället att driva nästa decennium av innovation inom CRISPR-teknik," sa de. "Genom att fortsätta utforska den naturliga världen kommer vi att upptäcka det som inte går att föreställa sig och använda det i verkligheten till förmån för planeten."
Image Credit: NIH
- SEO-drivet innehåll och PR-distribution. Bli förstärkt idag.
- Platoblockchain. Web3 Metaverse Intelligence. Kunskap förstärkt. Tillgång här.
- Källa: https://singularityhub.com/2023/01/25/crisprs-wild-first-decade-only-scratches-the-surface-of-its-potential/
- 2020
- a
- förmåga
- accelererad
- Acceptera
- noggrannhet
- uppnåendet
- handlingar
- Annat
- avancera
- avancerat
- framsteg
- första advent
- mot
- byråer
- dagordning
- Åldrande
- jordbruket
- framåt
- Syftet
- lindra
- ensam
- redan
- Även
- Alzheimers
- ammunition
- och
- djur
- djur
- godkänd
- områden
- Bistånd
- Författarna
- tillbaka
- bas
- Grunderna
- fördel
- Fördelarna
- Berkeley
- Bortom
- Stor
- Stora data
- Miljarder
- binda
- blod
- Direkt
- kropp
- lyft
- ökat
- Hjärna
- föra
- SLUTRESULTAT
- bygga förtroende
- Cancer
- kan inte
- Vid
- fall
- brottning
- Celler
- utmaningar
- chanser
- Förändringar
- byte
- billigare
- klassiska
- Klinisk
- kliniska tester
- koda
- färg
- kombination
- komma
- jämfört
- komponent
- omfattande
- komprometterande
- Konsekvenser
- konsortium
- konsumenter
- fortsätter
- kontroversiell
- konversationer
- kunde
- kredit
- Crispr
- kritisk
- grödor
- nyfikenhet
- För närvarande
- Klipp
- skärning
- datum
- årtionde
- Försvar
- leverera
- leverans
- utveckla
- Utveckling
- Upptäck
- Sjukdom
- sjukdomar
- DNA-
- ner
- dussintals
- drömmen
- driv
- drog
- under
- varje
- Tidig
- lätt
- redaktör
- effektivitet
- effekter
- effektivitet
- effektiv
- inkapslad
- ingenjör
- Teknik
- Går in
- speciellt
- etablerade
- upprättandet
- etisk
- Även
- utvecklas
- exempel
- expanderande
- utforska
- BERÖMMELSE
- gård
- SNABB
- FDA
- återkoppling
- bekämpa
- Förnamn
- Flexibilitet
- fokuserade
- livsmedel
- formen
- från
- full
- ytterligare
- framtida
- få
- allmänhet
- generera
- generering
- genteknik
- Genetik
- Välgörenhet
- Go
- Målet
- kommer
- uppgradera
- större
- riktlinjer
- Rubriker
- hälso-och sjukvård
- Hjärta
- hjälpa
- hjälper
- här.
- Hög
- Markera
- HTTPS
- humant
- Imaging
- Inverkan
- med Esport
- förbättra
- in
- Inklusive
- Öka
- ökat
- Ökar
- otroligt
- Innovation
- interaktioner
- Internationell
- IT
- Jennifer
- bara en
- Nyckel
- nycklar
- mördare
- Snäll
- kunskap
- storskalig
- leda
- inlärning
- låna
- brev
- livet
- linje
- längre
- du letar
- UTSEENDE
- Maskinen
- maskininlärning
- maskiner
- Huvudsida
- göra
- smink
- många
- mogen
- betyder
- mekanism
- metoder
- miljoner
- modeller
- modifierad
- Övervaka
- Månad
- mer
- mer effektiv
- mest
- rörliga
- mångfasetterad
- multipel
- Natural
- Natur
- Nära
- Behöver
- nervceller
- Nya
- Nästa
- NHS
- NIH
- Nobelpriset
- ökänd
- antal
- ONE
- ursprungliga
- Övriga
- Övrigt
- utanför
- Övervinna
- egen
- Papper
- Parallell
- Tidigare
- bana
- land
- Personer
- kanske
- planet
- Växter
- Plattformar
- plato
- Platon Data Intelligence
- PlatonData
- Massor
- befolkning
- möjlig
- potentiell
- potentiellt
- kraft
- den mäktigaste
- Praktisk
- Precision
- förutse
- förutsagda
- presenterar
- föregående
- tidigare
- Prime
- Priset
- problem
- Produkt
- ge
- allmän
- sätta
- snabbt
- nå
- når
- verklig
- verkliga världen
- Verkligheten
- senaste
- Red
- regulatorer
- frigöra
- förblir
- resterna
- kräver
- forskning
- forskare
- motståndskraft
- ansvaret
- Rik
- färdplan
- Roll
- Nämnda
- Vetenskap
- spana
- screening
- skärmar
- Andra
- in
- brist
- skall
- sida
- Tystnad
- Enkelt
- samtidigt
- eftersom
- enda
- webbplats
- Storlek
- Långsamt
- So
- Samhället
- några
- specifik
- fart
- Spot
- spunnen
- stadier
- Steg
- Fortfarande
- STEN
- strategier
- Struggles
- Kämpar
- student
- sådana
- lidande
- yta
- överleva
- Målet
- riktade
- targeting
- mål
- uppgift
- teknisk
- Teknologi
- Smakämnen
- Grunderna
- världen
- deras
- terapeutika
- tusentals
- tid
- gånger
- till
- i dag
- tillsammans
- Verktygslåda
- verktyg
- topp
- ämne
- Torn
- försök
- Litar
- SVÄNG
- typer
- UN
- underliggande
- förståelse
- uppdaterad
- användning
- olika
- mångsidig
- version
- välkommen
- Vad
- Vad är
- om
- som
- medan
- VEM
- Vild
- kommer
- beredd
- utan
- Vann
- Arbete
- fungerar
- världen
- år
- år
- Avkastning
- zephyrnet