Intuition och AI gör ett konstigt par.
Intuition är svår att beskriva. Det är den där magkänslan som gnager i dig, även om du inte vet varför. Vi bygger naturligt intuition genom erfarenhet. Magkänslorna är inte alltid rätt; men de kryper ofta in i vårt undermedvetna för att komplettera logik och resonemang när man fattar beslut.
AI däremot lär sig snabbt genom att smälta miljontals kalla, hårda datapunkter, och producerar rent analytiska – om inte alltid rimliga – resultat baserat på dess input.
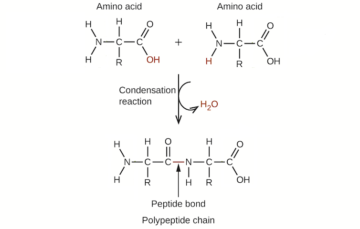
Nu, en ny studie in Nature Communications gifter sig med det udda paret, vilket resulterar i ett maskininlärningssystem som fångar en kemists intuition för läkemedelsutveckling.
Genom att analysera feedback från 35 kemister på Novartis, ett läkemedelsföretag baserat i Schweiz, utvecklade teamet en AI-modell som lär sig av mänsklig expertis i ett notoriskt svårt stadium av läkemedelsutveckling: att hitta lovande kemikalier som är kompatibla med vår biologi.
Först använde kemisterna sin intuition för att välja vilket av 5,000 XNUMX kemikaliepar som hade större chans att bli ett användbart läkemedel. Från denna feedback lärde sig ett enkelt artificiellt neuralt nätverk sina preferenser. När den utmanades med nya kemikalier gav AI-modellen var och en ett poäng som rankade om den var värd att utvecklas som medicin.
Utan några detaljer om själva de kemiska strukturerna fick AI "intuitivt" vissa strukturella komponenter, som ofta förekommer i befintliga mediciner, högre än andra. Överraskande nog fångade den också oklara egenskaper som inte explicit programmerats i tidigare datormodelleringsförsök. Parat med en generativ AI-modell, som DALL-E, designade robokemisten en mängd nya molekyler som potentiella leads.
Många lovande läkemedelskandidater var baserade på "kollativ kunskap", skrev teamet.
Studien är ett samarbete mellan Novartis och Microsoft Research AI4Science, den senare baserad i Storbritannien.
Nedför det kemiska kaninhålet
De flesta av våra vardagsmediciner är gjorda av små molekyler - Tylenol mot smärta, metformin för diabetesbehandling, antibiotika för att bekämpa bakterieinfektioner.
Men att hitta dessa molekyler är jobbigt.
Först måste forskarna förstå hur sjukdomen fungerar. Till exempel dechiffrerar de kedjan av biokemiska reaktioner som ger dig en bultande huvudvärk. Sedan hittar de den svagaste länken i kedjan, som ofta är ett protein, och modellerar dess form. Struktur i handen, de pekar ut skrymslen och vrår som molekyler kan fastna i för att störa proteinets funktion och därigenom sätta stopp för den biologiska processen – voilà, ingen mer huvudvärk.
Tack vare proteinförutsägelse AI, såsom AlphaFold, RoseTTAFold och deras utlöpare, är det nu lättare att modellera strukturen för ett målprotein. Att hitta en molekyl som passar den är en annan sak. Läkemedlet behöver inte bara ändra målets aktivitet. Det måste också lätt absorberas, spridas till målorganet eller vävnaden och säkert metaboliseras och elimineras från kroppen.
Det är här läkemedelskemister kommer in. Dessa vetenskapsmän är pionjärer i antagandet av datormodellering. För över två decennier sedan började fältet använda programvara för att sålla enormt stora databaser med kemikalier som letade efter lovande leads. Varje potentiell lead utvärderas sedan av ett team av kemister innan vidareutveckling.
Genom denna process bygger medicinska kemister en intuition som ger dem möjlighet att fatta beslut effektivt när man granskar lovande läkemedelskandidater. En del av deras träning kan vara destillerat till regler för datorer att lära sig – till exempel kommer denna struktur sannolikt inte att passera in i hjärnan; att man kan skada levern. Dessa expertregler har hjälpt till med initial screening. Men än så länge kan inget program fånga subtiliteterna och krångligheterna i deras beslutsfattande, delvis för att kemisterna inte kan förklara det själva.
Jag har en känsla
Den nya studien försökte fånga det oförklarliga i en AI-modell.
Teamet rekryterade 35 expertkemister vid olika Novartis-centra runt om i världen, alla med olika expertis. Vissa arbetar med celler och vävnader, till exempel, andra med datormodellering.
Intuition är svår att mäta. Det är inte heller direkt pålitligt. Som en baslinje designade teamet ett spel för flera spelare för att bedöma om varje kemist var konsekvent i sina val och om deras val överensstämde med andras. Varje kemist visades 220 molekylpar och ställde en avsiktligt vag fråga. Föreställ dig till exempel att du är i en tidig virtuell screeningkampanj och vi behöver ett läkemedel som kan tas som ett piller – vilken molekyl skulle du föredra?
Målet var att minska övertänkande och få kemisterna att lita på sin intuition för vilken kemikalie som stannar och vilken som går. Denna uppställning skiljer sig från vanliga utvärderingar, där kemisterna kontrollerar specifika molekylära egenskaper med prediktiva modeller – det vill säga hårda data.
Kemisterna var konsekventa i sin egen bedömning, men höll inte alltid med varandra – troligen på grund av olika personliga erfarenheter. Men det fanns tillräckligt med överlappning för att bilda ett underliggande mönster som en AI-modell kunde lära sig av, förklarade teamet.
Därefter byggde de upp datamängden till 5,000 XNUMX molekylpar. Molekylerna, var och en märkt med information om dess struktur och andra egenskaper, användes för att träna ett enkelt artificiellt neuralt nätverk. Med träning justerade AI-nätverket ytterligare sitt inre arbete baserat på feedback från kemister, vilket så småningom gav varje molekyl ett betyg.
Som en förnuftskontroll testade teamet modellen på kemiska par som skiljer sig från dem i deras träningsdatauppsättning. När de ökade antalet träningsprover, sköt prestandan upp.
Medan tidigare datorprogram har förlitat sig på regler för vad som gör ett lovande läkemedel baserat på molekylär struktur, speglade den nya modellens poäng inte direkt någon av dessa regler. AI fångade en mer holistisk syn på en kemikalie – en helt annan inställning till läkemedelsforskning än den som används i klassisk robo-kemistmjukvara.
Med hjälp av AI screenade teamet sedan hundratals FDA-godkända läkemedel och tusentals molekyler från en kemisk databank. Även utan explicit utbildning extraherade modellen kemiska strukturer - kallade "fragment" - som är mer mottagliga för vidareutveckling som läkemedel. AI:s poängpreferenser matchade de för befintliga läkemedelsliknande molekyler, vilket tyder på att den hade förstått kärnan i vad som gör en potentiell lead.
Kemisk romans
Novartis är inte det första företaget som utforskar en kemisk romans mellan människa och robot.
Tidigare har läkemedelsföretaget Merck knackade också i sin interna expertis för att rangordna kemikalier för en önskvärd egenskap. Utanför branschen, ett lag vid University of Glasgow utforskade att använda intuitionsbaserade robotar för oorganiska kemiska experiment.
Det är fortfarande en liten studie, och författarna kan inte utesluta mänskliga villfarelser. Vissa kemister kanske väljer en molekyl baserat på personliga fördomar som är svåra att helt undvika. Men upplägget skulle kunna användas för att studera andra steg i läkemedelsupptäckten som är dyra att genomföra experimentellt. Och även om modellen är baserad på intuition, kan dess resultat stärkas av regelbaserade filter för att ytterligare förbättra dess prestanda.
Vi är i en era där maskininlärning kan designa tiotusentals molekyler, förklarade teamet. En assisterande AI-kemist, beväpnad med intuition, kan hjälpa till att begränsa kandidater i det kritiska tidiga stadiet av läkemedelsupptäckten, och i sin tur påskynda hela processen.
Image Credit: Eugenia Kozyr / Unsplash
- SEO-drivet innehåll och PR-distribution. Bli förstärkt idag.
- PlatoData.Network Vertical Generative Ai. Styrka dig själv. Tillgång här.
- PlatoAiStream. Web3 Intelligence. Kunskap förstärkt. Tillgång här.
- Platoesg. Kol, CleanTech, Energi, Miljö, Sol, Avfallshantering. Tillgång här.
- PlatoHealth. Biotech och kliniska prövningar Intelligence. Tillgång här.
- Källa: https://singularityhub.com/2023/11/03/how-to-give-ai-a-gut-feeling-for-which-molecules-will-make-the-best-drugs/
- :är
- :inte
- :var
- $UPP
- 000
- 220
- 35%
- a
- accelerera
- aktivitet
- justerat
- Antagande
- sedan
- överens
- AI
- också
- alltid
- an
- analys
- och
- Annan
- vilken som helst
- tillvägagångssätt
- ÄR
- beväpnad
- runt
- konstgjord
- AS
- Assistent
- At
- Försök
- Författarna
- undvika
- baserat
- Baslinje
- BE
- därför att
- passande
- innan
- började
- BÄST
- mellan
- förspänner
- biologi
- kropp
- Hjärna
- SLUTRESULTAT
- byggt
- men
- by
- Kampanj
- KAN
- kandidater
- fånga
- fångas
- fångar
- Celler
- Centers
- vissa
- kedja
- utmanade
- chans
- ta
- kemisk
- val
- Välja
- klassiska
- förkylning
- samverkan
- komma
- företag
- kompatibel
- fullborda
- fullständigt
- komponenter
- dator
- datorer
- konsekvent
- Däremot
- kunde
- Par
- kredit
- kritisk
- dalls
- skada
- datum
- datapunkter
- databaser
- årtionden
- Dechiffrera
- Beslutsfattande
- beslut
- beskriva
- Designa
- utformade
- detaljer
- utvecklade
- Utveckling
- Diabetes
- olika
- olika
- svårt
- direkt
- Upptäckten
- Sjukdom
- Störa
- inte
- inte
- ner
- drog
- Läkemedel
- varje
- Tidigare
- Tidig
- tidigt skede
- lättare
- lätt
- utslagen
- enormt
- tillräckligt
- Era
- utvärderade
- utvärderingar
- Även
- så småningom
- dagliga
- exakt
- exempel
- befintliga
- dyra
- erfarenhet
- Erfarenheter
- experiment
- expert
- expertis
- Förklara
- förklarade
- uttryckligen
- utforska
- utforskas
- långt
- Funktioner
- återkoppling
- känslor
- fält
- bekämpa
- filter
- hitta
- finna
- Förnamn
- För
- formen
- från
- fungera
- ytterligare
- ytterligare utveckling
- lek
- mätare
- gav
- generativ
- Generativ AI
- Ge
- Ge
- Målet
- Går
- fick
- hade
- sidan
- Hård
- Har
- huvudvärk
- hjälpa
- hjälpte
- högre
- helhetssyn
- Hur ser din drömresa ut
- How To
- Men
- HTTPS
- humant
- Hundratals
- if
- bild
- förbättra
- in
- ökat
- industrin
- infektioner
- informationen
- inledande
- ingång
- exempel
- avsiktligt
- in
- intrikat
- IT
- DESS
- bara
- Vet
- Large
- leda
- Leads
- LÄRA SIG
- lärt
- inlärning
- tycka om
- sannolikt
- LINK
- Lever
- Logiken
- du letar
- Maskinen
- maskininlärning
- gjord
- göra
- GÖR
- Framställning
- ledning
- matchas
- Materia
- mäta
- medicin
- mediciner
- läkemedel
- metformin
- Microsoft
- kanske
- miljoner
- modell
- modellering
- molekylär
- molekyl
- mer
- flerspelarläget
- måste
- smal
- Natur
- Behöver
- nät
- neurala
- neurala nätverk
- Nya
- Nästa
- NIH
- Nej
- Novartis
- nu
- antal
- of
- sänkt
- Ofta
- on
- ONE
- or
- Övriga
- Övrigt
- vår
- ut
- utanför
- över
- egen
- Smärta
- par
- parade
- par
- passera
- Mönster
- prestanda
- personlig
- Läkemedelsindustrin
- Picks
- pionjärer
- plato
- Platon Data Intelligence
- PlatonData
- poäng
- potentiell
- förutsägelse
- föredra
- preferenser
- föregående
- process
- producerande
- Program
- programmerad
- Program
- lovande
- egenskaper
- Protein
- rent
- Tryckande
- sätta
- fråga
- kanin
- rangordna
- rankad
- snabbt
- reaktioner
- minska
- reflektera
- pålitlig
- förlita
- forskning
- resulterande
- Resultat
- reviewing
- höger
- robotar
- romantik
- Regel
- regler
- på ett säkert sätt
- vetenskapsmän
- göra
- poäng
- screening
- inställning
- Forma
- skott
- visas
- Sålla
- Enkelt
- Small
- So
- än så länge
- Mjukvara
- några
- eftersträvas
- specifik
- spridning
- Etapp
- Steg
- Fortfarande
- Sluta
- konstigt
- strukturell
- struktur
- strukturer
- Läsa på
- sådana
- komplettera
- schweiz
- system
- tagen
- Målet
- grupp
- tiotals
- testade
- än
- den där
- Smakämnen
- Storbritannien
- världen
- deras
- Dem
- sig själva
- sedan
- Där.
- vari
- Dessa
- de
- detta
- de
- tusentals
- Genom
- till
- TOTALT
- Tåg
- Utbildning
- SVÄNG
- två
- Uk
- underliggande
- förstå
- universitet
- Begagnade
- med hjälp av
- vanliga
- olika
- utsikt
- Virtuell
- var
- we
- były
- Vad
- när
- om
- som
- medan
- Hela
- varför
- kommer
- med
- utan
- Arbete
- fungerar
- fungerar
- världen
- skulle
- skrev
- Om er
- zephyrnet