Вікова дегенерація жовтої плями (ВМД) є основною причиною сліпоти. Він починається у зовнішньому гематогенному бар’єрі сітківки (oBRB), утвореному пігментним епітелієм сітківки (RPE), мембраною Бруха та хоріокапіляром. Механізми ініціації та прогресування AMD все ще потребують кращого розуміння через відсутність фізіологічно відповідних моделей oBRB людини.
Дослідницька група Національного інституту ока (NEI), яка є частиною Національного інституту здоров’я, використовувала пацієнта Стовбурові клітини і 3D-біодрук для виробництва очної тканини, яка сприятиме розумінню механізмів сліпих хвороб. Вчені надрукували комбінацію клітин, які утворюють зовнішній гемато-сітківковий бар’єр.
Пігментний епітелій сітківки (RPE), відокремлений від багатого кровоносними судинами хоріокапіляра мембрана Бруха, утворює зовнішній гемато-сітківковий бар’єр. Хоріокапілляр і РПЕ обмінюються поживними речовинами та відходами під контролем мембрани Бруха. Друзи, які є скупченнями ліпопротеїдів, розвиваються поза мембраною Бруха при ВМД і перешкоджають її функціонуванню. Деградація RPE з часом спричиняє погіршення роботи фоторецепторів і втрату зору.
Вчені об’єднали в гідрогель три типи незрілих хоріоїдальних клітин: перицити, ендотеліальні клітини та фібробласти. Потім вони надрукували гель на біорозкладаному каркасі. За кілька днів клітини почали дозрівати в густу капілярну мережу.
На дев'ятий день вчені посіяли пігментні епітеліальні клітини сітківки на зворотному боці шафоту. Надрукована тканина досягла повної зрілості на 42-й день. Аналіз тканини, генетичне та функціональне тестування показали, що надрукована тканина виглядала та поводилася подібно до природного зовнішнього гемато-сітківкового бар’єру.
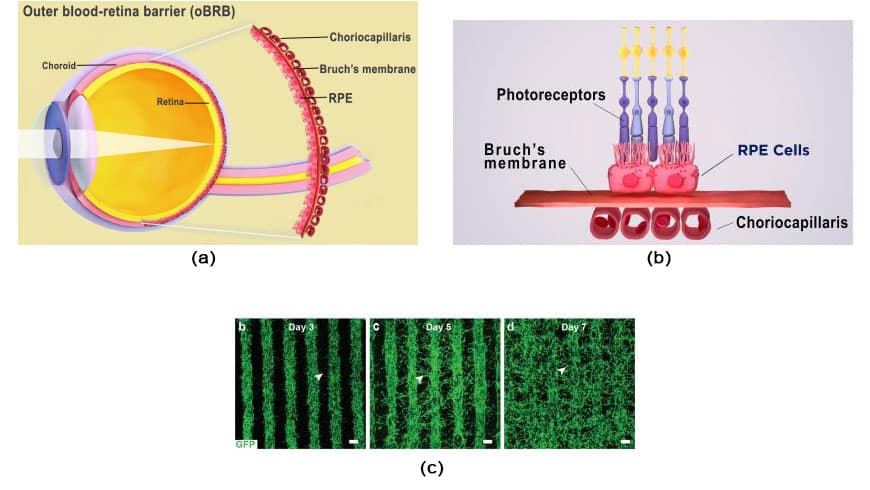
b. Зовнішній гемато-сітківковий бар’єр ока складається з пігментного епітелію сітківки, мембрани Бруха та хоріокапіляра. Кредит зображення: Національний інститут ока.
в. Ріст кровоносних судин через надруковані ряди суміші ендотеліальних, перицитних і фібробластних клітин. До 7 дня кровоносні судини заповнюють простір між рядами, утворюючи мережу капілярів. Кредит зображення: Kapil Bharti.
Під впливом стресу надрукована тканина демонструвала характеристики ранньої стадії ВМД, такі як відкладення друз під РПЕ, і прогресувала до пізньої стадії сухої стадії ВМД, де спостерігалося руйнування тканини. Низький рівень кисню викликав вологий вигляд, подібний до ВМД, з гіперпроліферацією хоріоїдальних судин, яка перемістилася в зону суб-RPE. При використанні для лікування ВМД препарати проти VEGF уповільнюють утворення та міграцію кровоносних судин, а також покращують форму тканин.
Капіл Бхарті, доктор філософії, який очолює відділ NEI з досліджень трансляції очей і стовбурових клітин, сказав: «Друкуючи клітини, ми сприяємо обміну клітинними сигналами, необхідними для нормальної анатомії зовнішнього гемато-сітківкового бар’єру. Наприклад, наявність клітин RPE індукує експресії генів зміни у фібробластах, які сприяють формуванню мембрани Бруха — те, що було запропоновано багато років тому, але не було доведено до нашої моделі».
Вчені розглянули дві технологічні проблеми: створення відповідного біорозкладаного каркасу та досягнення узгодженого візерунка друку. Вони розробили чутливий до температури гідрогель, який створював чіткі ряди, поки гель був холодним, але розчинявся, коли гель нагрівався. Більш точна система оцінки архітектури тканини стала можливою завдяки хорошій послідовності рядів. Крім того, вони оптимізували пропорцію фібробластів, ендотеліальних клітин і перицитів у комбінації клітин.
Співавтор Марк Феррер, доктор філософії, директор лабораторії 3D біодруку тканин у Національному центрі розвитку трансляційних наук NIH, і його команда надали досвід біофабрикації зовнішніх тканин бар’єру «кров-сітківка» «в лунці, ” разом з аналітичними вимірюваннями, щоб уможливити скринінг наркотиків.
[Вбудоване вміст]
«Наші спільні зусилля призвели до дуже актуальних моделей тканини сітківки ока для дегенеративних захворювань очей», — Феррер сказав. «Такі моделі тканин мають багато потенційних застосувань у трансляційних програмах, включаючи розвиток терапії».
Довідка з журналу:
- Мін Дже Сонг, Расс Квінн та ін. Біодрукований 3D-зовнішній бар’єр сітківки розкриває RPE-залежний хоріоїдальний фенотип при поширеній дегенерації жовтої плями. Методи природи2022; DOI: 10.1038/s41592-022-01701-1