年龄相关性黄斑变性(AMD)是导致失明的主要原因。 它起始于由视网膜色素上皮 (RPE)、布鲁赫膜和脉络膜毛细血管形成的外血视网膜屏障 (oBRB)。 由于缺乏生理相关的人类 oBRB 模型,AMD 的启动和进展机制仍然需要更好地理解。
美国国立卫生研究院下属的国家眼科研究所 (NEI) 研究小组使用患者 干细胞 通过 3D 生物打印来生产眼组织,这将促进对致盲疾病机制的理解。 科学家打印了形成外血视网膜屏障的细胞组合。
视网膜色素上皮 (RPE) 通过以下方法与富含血管的脉络膜毛细血管分离 布鲁赫膜,构成外层血视网膜屏障。 脉络膜毛细血管和视网膜色素上皮在布鲁赫膜的控制下交换营养物质和废物。 玻璃疣是脂蛋白积聚物,在 AMD 的布鲁赫膜外生长并阻碍其功能。 随着时间的推移,RPE 退化会导致光感受器退化和视力丧失。
科学家将三种未成熟的脉络膜细胞类型组合在水凝胶中:周细胞、内皮细胞和成纤维细胞。 然后他们将凝胶打印在可生物降解的支架上。 几天之内,细胞开始成熟为致密的毛细血管网络。
第九天,科学家们将视网膜色素上皮细胞接种到支架的另一侧。 打印的组织在第 42 天达到完全成熟。组织分析以及遗传和功能测试表明,打印的组织的外观和行为与天然外血视网膜屏障相似。
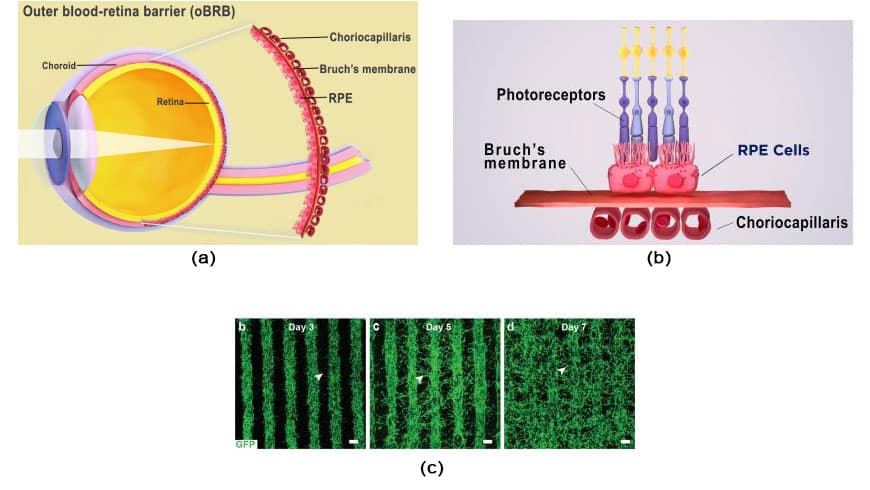
b. 眼睛的外血视网膜屏障包括视网膜色素上皮、布鲁赫膜和脉络膜毛细血管。 图片来源:国家眼科研究所。
C。 血管在打印的内皮-周细胞-成纤维细胞混合物行中生长。 到了第 7 天,血管充满了各行之间的空间,形成毛细血管网络。 图片来源:卡皮尔·巴蒂。
当受到压力时,打印的组织表现出早期 AMD 特征,例如视网膜色素上皮下的玻璃膜疣沉积,并发展到晚期干性 AMD,出现组织破裂。 低氧水平导致湿性 AMD 样外观,脉络膜血管过度增殖并移至 RPE 下区域。 当用于治疗 AMD 时,抗 VEGF 药物可以减缓血管的形成和迁移,同时改善组织形状。
NEI 眼部和干细胞转化研究部门负责人 Kapil Bharti 博士表示, “通过打印细胞,我们正在促进正常外血视网膜屏障解剖结构所需的细胞线索的交换。 例如,RPE 细胞的存在会诱导 基因表达 成纤维细胞的变化有助于布鲁赫膜的形成——很多年前就有人提出这一点,但直到我们的模型才得到证实。”
科学家们解决了两个技术问题:创建合适的可生物降解支架和实现一致的印刷图案。 他们开发了一种温度敏感的水凝胶,当凝胶冷时会产生明显的行,但当凝胶变暖时会溶解。 良好的行一致性使得更精确的组织结构评估系统成为可能。 此外,他们还优化了细胞组合中成纤维细胞、内皮细胞和周细胞的比例。
共同作者 Marc Ferrer 博士是 NIH 国家推进转化科学中心 3D 组织生物打印实验室主任,他的团队为“在孔中、 ”以及分析测量以实现药物筛选。
[嵌入的内容]
“我们的合作努力已经产生了与退行性眼病非常相关的视网膜组织模型,”费雷尔 说过。 “此类组织模型在转化应用中具有许多潜在用途,包括疗法开发。”
杂志参考:
- Min Jae Song、Russ Quinn 等人。 生物打印 3D 外视网膜屏障揭示了晚期黄斑变性中 RPE 依赖性脉络膜表型。 自然方法,2022; DOI: 10.1038/s41592-022-01701-1