Aldersrelatert makuladegenerasjon (AMD) er en ledende årsak til blindhet. Det starter i den ytre blod-retina-barrieren (oBRB) dannet av retinalt pigmentepitel (RPE), Bruchs membran og choriocapillaris. AMD-initierings- og progresjonsmekanismer må fortsatt forstås bedre på grunn av mangelen på fysiologisk relevante menneskelige oBRB-modeller.
The National Eye Institute (NEI) forskerteam, en del av National Institutes of Health, brukte pasient stamceller og 3D bioprinting for å produsere øyevev som vil fremme forståelsen av mekanismene til blendende sykdommer. Forskere trykket en kombinasjon av celler som danner den ytre blod-retina-barrieren.
Det retinale pigmentepitelet (RPE), separert fra den blodkarrike choriocapillaris ved Bruchs membran, utgjør den ytre blod-retina-barrieren. Choriocapillaris og RPE utveksler næringsstoffer og avfall under kontroll av Bruchs membran. Drusen, som er lipoproteinansamlinger, utvikles utenfor Bruchs membran ved AMD og hindrer dens funksjon. RPE-nedbrytning over tid forårsaker fotoreseptorforringelse og synstap.
Forskere kombinerte tre umodne koroidale celletyper i en hydrogel: pericytter, endotelceller og fibroblaster. De trykket deretter gelen på et biologisk nedbrytbart stillas. I løpet av dager begynte cellene å modnes til et tett kapillærnettverk.
På dag ni så forskerne retinale pigmentepitelceller på baksiden av stillaset. Det trykte vevet nådde full modenhet på dag 42. Vevsanalyser og genetiske og funksjonelle tester viste at det trykte vevet så ut og oppførte seg på samme måte som den naturlige ytre blod-retina-barrieren.
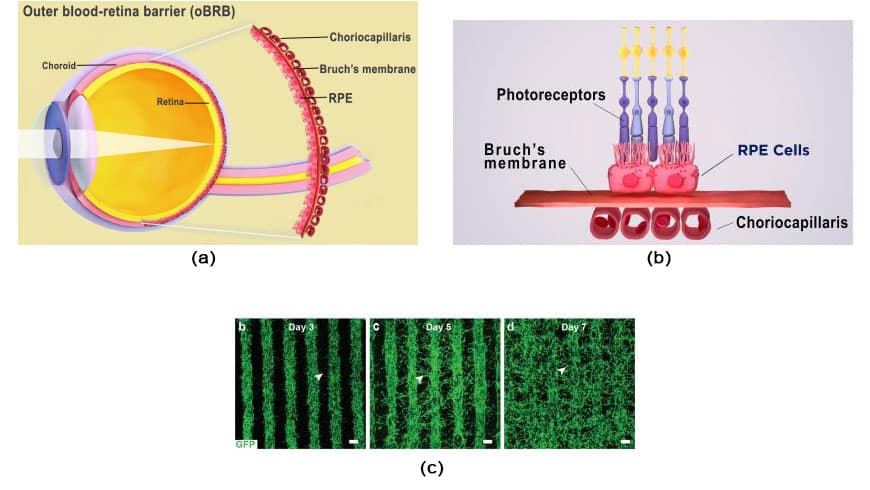
b. Øyets ytre blod-retina-barriere omfatter retinalt pigmentepitel, Bruchs membran og choriocapillaris. Bildekreditt: National Eye Institute.
c. Vekst av blodårer over trykte rader av en endotel-pericytt-fibroblastcelleblanding. På dag 7 fyller blodkar ut rommet mellom radene, og danner et nettverk av kapillærer. Bildekreditt: Kapil Bharti.
Når det ble utsatt for stress, viste trykt vev AMD-karakteristikker i tidlig stadium, slik som drusenavleiringer under RPE, og gikk videre til sent stadium i tørt stadium AMD, hvor vevsnedbrytning ble sett. Lave oksygennivåer forårsaket et vått AMD-lignende utseende med koroidal vaskulær hyperproliferasjon som beveget seg inn i sub-RPE-sonen. Når de ble brukt til å behandle AMD, bremset anti-VEGF-medisiner dannelsen og migrasjonen av blodkar, samtidig som de forbedret vevsformen.
Kapil Bharti, Ph.D., som leder NEI-seksjonen for okulær og stamcelle-translasjonsforskning sa: "Ved å skrive ut celler, letter vi utvekslingen av cellulære signaler som er nødvendige for normal ytre blod-retina-barriere-anatomi. For eksempel induserer tilstedeværelsen av RPE-celler genuttrykk endringer i fibroblaster som bidrar til dannelsen av Bruchs membran - noe som ble foreslått for mange år siden, men som ikke ble bevist før vår modell."
Forskere tok for seg to teknologiske problemer: å lage et passende biologisk nedbrytbart stillas og å oppnå et konsistent utskriftsmønster. De utviklet en temperaturfølsom hydrogel som produserte distinkte rader mens gelen var kald, men oppløst når gelen ble varmet. Et mer nøyaktig system for vurdering av vevsarkitektur ble muliggjort av god radkonsistens. I tillegg optimaliserte de andelen fibroblaster, endotelceller og pericytter i cellekombinasjonen.
Medforfatter Marc Ferrer, Ph.D., direktør for 3D Tissue Bioprinting Laboratory ved NIHs National Center for Advancing Translational Sciences, og teamet hans ga ekspertise for biofabrikasjon av det ytre blod-retina-barrierevevet "i-en-brønn, ” sammen med analytiske målinger for å muliggjøre medikamentscreening.
[Innebygd innhold]
"Vår samarbeid har resultert i svært relevante netthinnevevsmodeller av degenerative øyesykdommer," Ferrer sa. "Slike vevsmodeller har mange potensielle bruksområder i translasjonsapplikasjoner, inkludert terapeutisk utvikling."
Tidsreferanse:
- Min Jae Song, Russ Quinn et al. Bioprintet 3D ytre retinabarriere avdekker RPE-avhengig koroidal fenotype i avansert makuladegenerasjon. Naturmetoder, 2022; GJØR JEG: 10.1038/s41592-022-01701-1